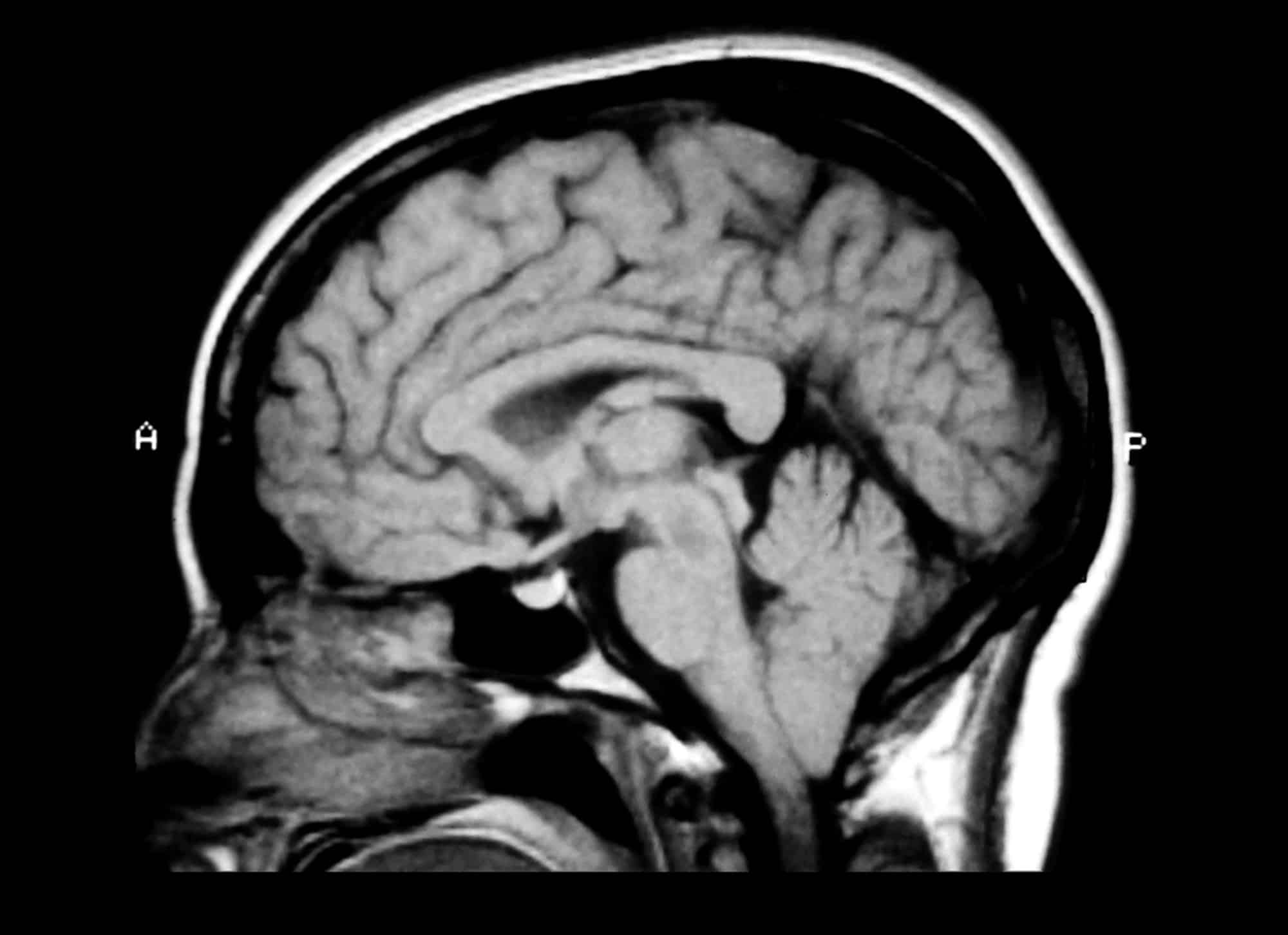
L’intérêt scientifique pour la malformation de Chiari (CM), également connue sous le nom de malformation d’Arnold-Chiari, est élevé. Depuis le début de 2016 jusqu’à aujourd’hui, PubMed a indexé 309 articles publiés, soit une moyenne de 2,25 par semaine. Cependant, comme la CM est une maladie rare, la plupart des études publiées sont rétrospectives et basées sur de petits nombres. Les méta-analyses sont seulement aussi bonnes que la qualité des données primaires, qui sont généralement des preuves faibles à moyennes dans le cas de CM. Cela ne fait pas grand-chose pour remédier à la confusion généralisée autour de la CM et de son traitement.
Définition de la malformation de Chiari
A voir aussi : Comment formuler une demande d’aide juridictionnelle à la CNDA ?
Le périmètre actuel de la CM reste trop vaste pour être précis. En 1891, Hans Chiari a posé les bases en distinguant trois formes de malformations caractérisées par une hernie du cerveau postérieur hors du crâne :
- Le type I, où les amygdales cérébelleuses s’engagent dans le canal rachidien à travers le foramen magnum sur au moins 5 mm.
- Le type II, qui implique le tronc cérébral et le cervelet (y compris le quatrième ventricule), toujours associé à un myéloméningocèle.
- Le type III, où l’on observe une encéphalocèle contenant le cervelet.
Un quatrième type a été ajouté par la suite : il correspond à une hypoplasie, voire une absence complète du cervelet, sans hernie associée.
A lire aussi : Purepeople face à ses concurrents : quelles alternatives privilégier ?
Certains chercheurs évoquent aussi des sous-types 0 et 1,5, mais ces catégories demeurent controversées. D’autres auteurs incluent même des situations où la hernie du cerveau postérieur ne découle pas d’une anomalie congénitale, mais d’une pathologie intracrânienne comme une tumeur ou une hydrocéphalie.
Ici, seul le type I (CM-I) retient notre attention. Il s’agit de la forme la plus fréquente, caractérisée par une descente des amygdales cérébelleuses dans le canal rachidien, souvent sur fond de fosse postérieure exiguë. Les manifestations varient énormément, car la zone concernée regorge de noyaux nerveux essentiels : noyau vagal, nerfs oculomoteurs, noyaux du trijumeau, nerf facial, innervation de la langue… Le cervelet, quant à lui, intervient dans la coordination, l’équilibre, mais aussi dans certains aspects cognitifs.
Symptômes de la CM
Les signes neurologiques peuvent apparaître dès la naissance, plus tard dans l’enfance, ou même à l’âge adulte. Beaucoup de personnes atteintes de CM-I ne présentent aucun symptôme et peuvent l’ignorer longtemps. Parfois, la compression du tronc cérébral ou du cervelet provoque des douleurs cervicales, des vertiges, des acouphènes, des troubles de la parole ou de la déglutition, des épisodes d’apnée du sommeil, des nausées, des vomissements, ou encore un manque de coordination des mains, y compris dans les gestes les plus fins.
La céphalée, symptôme le plus courant de la CM-I, s’explique par une perturbation de la circulation du liquide céphalo-rachidien (LCR) au niveau du foramen magnum. Cette douleur s’aggrave nettement lors des accès de toux. Lorsque le LCR circule mal, il peut provoquer une hydromyélie (dilatation du canal médullaire) ou une syringomyélie (cavités remplies de liquide dans la moelle épinière). Ces complications nuisent à la fonction médullaire, entraînant faiblesse musculaire ou troubles de la sensibilité. Devant de tels symptômes, il est indispensable de recourir à une IRM du cerveau et de toute la colonne vertébrale pour rechercher une éventuelle syringomyélie.
Par ailleurs, des travaux récents font état de troubles cognitifs chez certains patients porteurs de CM. Un examen approfondi montre que les difficultés touchant les fonctions exécutives sont plus documentées que d’autres altérations des capacités mentales. Toutefois, ces résultats appellent à des études prospectives plus solides pour confirmer la réalité de ce lien.
Prise en charge de la CM
Pour les formes symptomatiques de CM-I, la chirurgie s’impose, avec pour objectif de lever la compression et de restaurer un écoulement normal du LCR. Le nombre d’interventions continue de croître, même si la chirurgie préventive n’est pas recommandée chez les patients asymptomatiques. Oliver Bozinov, chef de service à l’hôpital universitaire de Zurich, alerte sur la tendance à opérer trop rapidement, parfois par manque d’expérience, avec un risque accru de complications postopératoires.
Articles connexes
- Résultats positifs pour Soliris in Neuromyelitis Optica Spectrum Disorder Trial
- Des dizaines de groupes médicaux unissent leurs forces pour améliorer les diagnostics
- Les hôpitaux facturent 479 pourcent du coût des médicaments en moyenne
Les éléments disponibles indiquent que les patients sans symptômes doivent être rassurés : la probabilité de développer des troubles neurologiques reste faible. Un suivi régulier par IRM demeure la meilleure stratégie. Une méta-analyse récente, qui a suivi des asymptomatiques sur plus de dix ans, a révélé que plus de 93 % d’entre eux, y compris certains avec syringomyélie, n’avaient pas vu leur état se modifier au fil du temps. Chez les personnes présentant des maux de tête ou des nausées, une surveillance attentive, parfois accompagnée d’un traitement symptomatique, peut suffire. Cette démarche prudente limite les risques liés à une chirurgie inutile.
L’opération devient incontournable en cas d’atteintes graves : gêne des nerfs crâniens, signes cérébelleux, myélopathie, syringomyélie avérée ou céphalée de toux insupportable. La plupart des neurochirurgiens réalisent une décompression de la fosse postérieure, par craniectomie suboccipitale et laminectomie de la première vertèbre cervicale. Pour un effet maximal, la dure-mère est souvent incisée, puis élargie à l’aide d’un patch (tissu du patient ou matériel synthétique).
Une méta-analyse récente a comparé deux approches : laisser la dure-mère intacte réduit la durée opératoire, mais diminue les chances d’amélioration postopératoire de 15 %. Pratiquer une duraplastie prolonge la chirurgie et expose à davantage de fuites de LCR, mais offre de meilleurs résultats sur le plan clinique, notamment pour traiter la syringomyélie. Si une syringomyélie symptomatique persiste, il est possible de poser un shunt pour drainer le liquide vers d’autres espaces corporels. Parmi les complications postopératoires, on recense la méningite, les hématomes, l’apnée et divers troubles du tronc cérébral, qui restent heureusement rares mais sérieux.
Chez l’enfant, une alternative consiste parfois en une simple incision de la dure-mère, sans correction supplémentaire, avec des résultats encourageants. Une technique plus récente, l’amygdalectomie cérébelleuse sous-piale minimalement invasive, associée à une reconstruction du cisterna magna, a aussi été proposée comme alternative. Toutefois, certains spécialistes mettent en garde contre le risque d’arachnoïdite et de formation d’adhérences après ce geste, susceptibles de dégrader la récupération. À noter : malgré une décompression bien menée, il n’est pas exclu que la maladie progresse encore chez quelques patients.
En règle générale, le pronostic après l’opération reste globalement favorable, mais dépend fortement de la gravité initiale. Les patients souffrant de troubles neurologiques anciens ou d’atrophie musculaire peuvent garder des séquelles. Finalement, la CM-I demeure un défi pour les neurochirurgiens, qui doivent adapter finement leur stratégie aux particularités de chaque personne.
Références
- Institut national des troubles neurologiques et des accidents vasculaires cérébraux. Fiche d’information sur la malformation de Chiari. https://www.ninds.nih.gov/Disorders/Patient-Caregiver-Education/Fact-Sheets/Chiari-Malformation-Fact-Sheet. Mis à jour le 6 juillet 2018. Consulté le 20 août 2018.
- Langridge B, Phillips E, Choi D. Chiari malformation type 1 : revue systématique de l’histoire naturelle et gestion conservatrice. World Neurosurg. 2017 ; 104:213,219.
- Gad, KA, Yousem, SM. Syringohydromyélie chez les patients atteints de malformation de Chiari I : analyse rétrospective. AJNR Am J Neuroradiol.2017 ; 38:1833 -1838.
- Rogers J.M., Savage G, Stoodley MA. Un examen systématique de la cognition dans la malformation de Chiari I. Neuropsychol Rev. 2018 ; 28:176 -187.
- Wilkinson DA, Johnson K, Garton HJL, Muraszko KM, Maher CO. Tendances dans le traitement chirurgical de la malformation de Chiari Type I aux États-Unis. J Neurosurg Pediatr. 2017 ; 19:208 -216.
- Xu H, Chu L, He R, Ge C, Lei T. Décompression de la fosse postérieure avec et sans duraplastie pour le traitement de la malformation de Chiari type I-A revue systématique et méta-analyse. Neurosurg Rév. 2017 ; 40:213 -221.
- Bhimani AD, Esfahani R.D., Denyer S, et coll. Malformations Chiari I adultes : analyse des facteurs de risque et des complications chirurgicales à l’aide d’une base de données internationale. Monde Neurosurg. 2018 ; 115:e490-e500.
- Kurzbuch AR, Jayamohan J, Magdum S. Traitement chirurgical de la malformation pédiatrique Chiari I : décompression foramen magnum avec dura laissée ouverte, chez 70 patients. Présenté au : Symposium international Syringomyelia-Chiari 2018 ;17-20 juillet 2018 ; Birmingham, Royaume-Uni.
- Lou Y, Li H, Jin Y, Liu L. Amyillectomie sous-piale minimalement invasive (MIST) et reconstruction de la cysterna magna dans le traitement de la malformation de Chiari type 1 par syringomyélie. Présenté à : Syringomyelia-Chiari 2018 International Symposium ; 17-20 juillet 2018 ; Birmingham, Royaume-Uni.
Face à la CM-I, chaque prise en charge devient un véritable parcours singulier, où le pari du sur-mesure l’emporte sur la standardisation. Les avancées récentes laissent entrevoir de nouvelles pistes, mais les défis, eux, ne se laissent pas oublier : c’est là tout l’enjeu pour les années à venir.